إنتاج كبريتيد الهيدروجين وخصائصه وتطبيقه
في هذه المقالة سننظر في إنتاج كبريتيد الهيدروجين من الكبريت. دعونا نلقي نظرة فاحصة على الخصائص الفيزيائية والكيميائية لهذه المادة.

هيكل
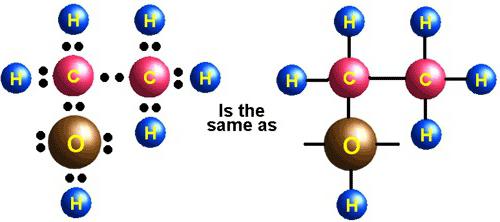
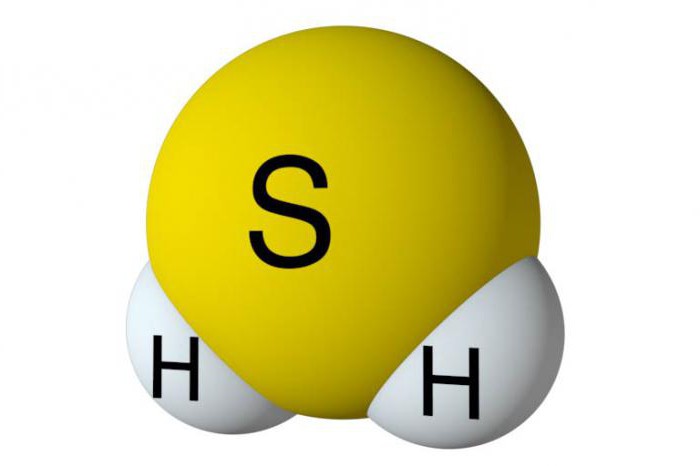
من أجل تحليل الرئيسياستقبال كبريتيد الهيدروجين ، فمن الضروري معرفة خصوصيات هيكلها. تحتوي هذه المادة على ذرة كبريت واثنين من الهيدروجين. فهي غير اللافلزية ، وتشكل روابط قطبية تساهمية بين العناصر. يوجد في كبريتيد الهيدروجين بنية زاويّة. بين الكبريت والهيدروجين ، يتم تشكيل زاوية 92 درجة ، وهو أقل بقليل من الماء.
الخصائص الفيزيائية
رائحة كبريتيد الهيدروجين ، تذكرنا بالبيض الفاسد ،مألوف للجميع. في ظل الظروف العادية ، تكون هذه المادة في الحالة الغازية. لا يوجد لديه لون ، وقابل للذوبان في الماء سيئة ، سامة. في المتوسط ، عند 20 درجة مئوية ، سوف يذوب 2.4 مجلد من كبريتيد الهيدروجين في الماء. في المياه الكبريتية ، يتم الكشف عن خصائص حمضية طفيفة ، ويتوقف تفكك المادة تدريجياً. كبريتيد الهيدروجين السام خطير حتى في الجرعات الصغيرة. يؤدي المحتوى المحمول جواً بنسبة 0.1٪ من كبريتيد الهيدروجين إلى شلل مركز الجهاز التنفسي مع فقدان الوعي. على سبيل المثال ، توفي عالم الطبيعة الأسطوري بليني الأكبر في القرن التاسع قبل الميلاد بالضبط من كبريتيد الهيدروجين ، الذي تشكل أثناء ثوران فيزوف.
سبب تأثير التسمم من كبريتيد الهيدروجين في تفاعلها الكيميائي مع الهيموجلوبين في الدم. يشكل الحديد الموجود في هذا البروتين كبريتيد مع كبريتيد الهيدروجين.
أقصى تركيز مسموح به في الهواءيعتبر كبريتيد الهيدروجين 0.01 مغ / ل. كترياق ، يتم استخدام استنشاق الأكسجين النقي أو الهواء ، الذي يوجد فيه كمية غير كافية من الكلور.
العمل مع كبريتيد الهيدروجين يعني الالتزام ببعض قواعد السلامة. تتم جميع التجارب التي تنطوي على هذه المادة الغازية في أجهزة مختومة وغطاسات الدخان.

طرق لإنتاج كبريتيد الهيدروجين
ما هو إنتاج كبريتيد الهيدروجين في المختبر؟ الخيار الأكثر شيوعا هو تفاعل الهيدروجين مع الكبريت. يشير هذا التفاعل الكيميائي إلى مركب يتم إجراؤه في غطاء الدخان.
بالإضافة إلى ذلك ، يمكن إنتاج كبريتيد الهيدروجين أيضًاالتبادل بين كبريتيد الحديد الصلب (2) ومحلول حمض الكبريتيك أو الهيدروكلوريك. للحصول على هذه النتيجة ، يكفي أخذ بضع قطع من الكبريتيد في أنبوب اختبار لا يتجاوز حجم البازيلاء. علاوة على ذلك ، يضاف محلول الحمض إلى الأنبوب (حتى نصف الحجم) ، المغطى بأنبوب مخرج الغاز. يتم وضع الجهاز تحت غطاء المحرك ، يتم تسخين الأنبوب. التفاعل الكيميائي يرافقه إطلاق فقاعات غازية. هذا الإنتاج من كبريتيد الهيدروجين يسمح بإنشاء كمية من مادة كافية للنظر في خصائصه الكيميائية.
ما هي الطرق الأخرى هناك؟ يسمح المختبر بإنتاج كبريتيد الهيدروجين من خلال تفاعل الحديد المعدني (تحت غطاء المحرك) مع الكبريت البلوري ، متبوعًا بتفاعل كبريتيد مع حمض الكبريتيك.

الخصائص الكيميائية
يتفاعل كبريتيد الهيدروجين مع الأكسجين في الهواء ،يحترق بلون مزرق. في حالة الاحتراق الكامل ، تكون منتجات التفاعل عبارة عن أكسيد الكبريت (4) والماء. وبالنظر إلى أن غاز الفرن هو أكسيد حامضي ، فإنه في المحلول يشكل حمض كبريتي ضعيف ، مما يلوث ورقة عباد الشمس باللون الأحمر.
في حالة وجود كمية غير كافية من كبريتيد الهيدروجين ، يتم تكوين الكبريت البلوري. تعتبر هذه العملية طريقة صناعية للحصول على الكبريت النقي من كبريتيد الهيدروجين.
هذه المادة الكيميائية قد تم تحديدها والقدرات التصالحية ممتازة. تتجلى ، على سبيل المثال ، عند التفاعل مع الأملاح ، الهالوجينات. من أجل إجراء تفاعل مماثل تحت ظروف المختبر ، يتم صب محلول من كبريتيد الهيدروجين في أنابيب الاختبار مع الكلور والبروم ، ويلاحظ تغير اللون. كمنتج التفاعل ، لوحظ تشكيل الكبريت البلورية.
التفاعل الكيميائي لكبريتيد الهيدروجين مع الماء يؤدي إلى تكوين الكاتيون الهيدروجينى H3O +.
كبريتيد الهيدروجين قادر على تكوين نوعين من المركبات: كبريتيد (أملاح متوسطة) وهيدروسلفيدات (أملاح حمضية).
في معادن الأرض القلوية والقلوية ، الكبريتيداتهي مركبات عديمة اللون. في المعادن الثقيلة (النحاس والنيكل والرصاص) هم من السود. كبريتيد المنغنيز له لون وردي. العديد من الأملاح لا تذوب في الماء.
رد فعل نوعي للكبريتيدات هو التفاعل مع محلول كبريتات النحاس (2). ناتج هذا التفاعل هو ترسيب راسب أسود من كبريتيد النحاس (2).
استنتاج
في الطبيعة هذه المادة موجودة في المعادنمصادر الغازات البركانية. هذا المركب هو نتاج تحلل الحيوانات والكائنات النباتية ، ويتميز برائحة مميزة من كبريتيد الهيدروجين. تم العثور على الكبريتيدات الطبيعية في تكوين المعادن النادرة ، في علم المعادن منها يتم الحصول على العناصر المقابلة. من المهم أيضا أن نتذكر أن كبريتيد الهيدروجين هو سم قوي.